انطلاق تطبيق أول علاج جيني لأمراض الدم في بريطانيا
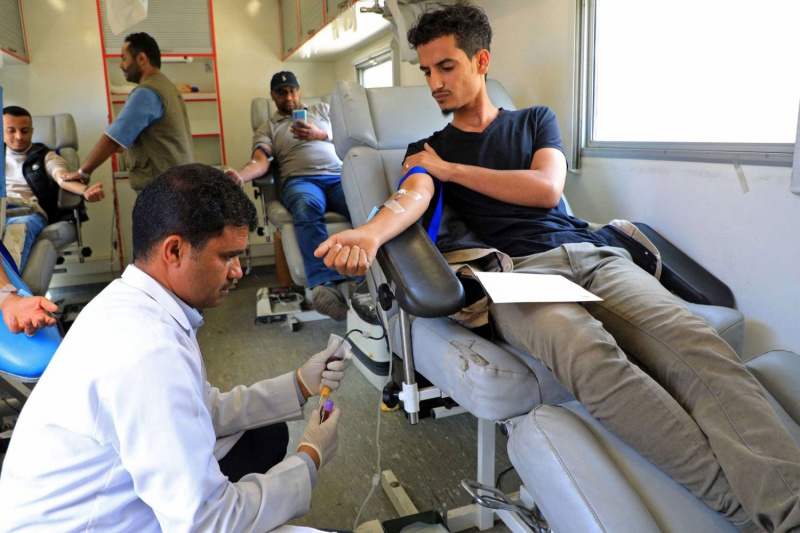
يؤكد خبراء الصحة في بريطانيا أن علاج "كاسجيفي" يحمل آمالًا كبيرة لمرضى الثلاسيميا وفقر الدم المنجلي، وفوائد طويلة الأمد يمكن أن تحسن حياتهم بشكل كبير، حيث يقلل من حاجتهم إلى عمليات نقل الدم. كما أن عوارضه الجانبية أخف من عوارض العلاجات السابقة. ويوجه "كاسجيفي" الجسم لإنتاج الهيموجلوبين الذي يسمح لخلايا الدم الحمراء بنقل الأوكسجين إلى جميع أنحاء الجسم.
لندن - شرعت بريطانيا في تطبيق أول علاج جيني (كاسجيفي) لأمراض الدم والذي يهم مرضى “الثلاسيميا” من نوع “بيتا” وفقر الدم المنجلي، على 460 شخصا بعد أن أعلنت على حصولها على ترخيص كأول علاج منذ سنة.
وتتمثل تقنية “كاسيجيفي” في قيام الأطباء باستخراج الخلايا الجذعية من نخاع المريض العظمي، ثم تعدل الجينات في مختبر باستخدام تكنولوجيا “كريسبر”، ليتم حقن الجينات المعدلة مرة أخرى في المريض، وبالتالي يمكنها أن توجه الجسم لإنتاج الهيموجلوبين الذي يسمح لخلايا الدم الحمراء بنقل الأكسجين في جميع أنحاء الجسم.
وبحسب رئيس المكتب الطبي في المعهد الوطني للصحة والبحوث التطبيقية البروفيسور جوناثان بينغر فإن العلاج يحمل آمالًا كبيرة، وفوائد طويلة الأمد يمكن أن تحسن حياة المريض بشكل كبير، فهو يقلل من حاجة المرضى إلى عمليات نقل الدم. كما أن عوارضه الجانبية أخف من عوارض العلاجات السابقة، إذ يقول البروفيسور جون بورتر إن العلاجات السابقة لم تستطع أن تحد من المشاكل التي يعاني منها مرضى الثلاسيميا كهشاشة العظام وتليف الكبد، وغيرها، لكن هذه المرة يتأملون أن “يتم التخلص من تلك المضاعفات”.
ويعد مرض الثلاسيميا من أكثر الأمراض شيوعا في العالم، خاصة في أفريقيا وحوض البحر الأبيض المتوسط. والثلاسيميا هو اضطراب دم وراثي يؤدي إلى انخفاض نسبة الهيموغلوبين في الجسم عن المعدل الطبيعي ويمكن الهيموغلوبين خلايا الدم الحمراء من حمل الأكسجين وقد تتسبب الثلاسيميا في فقر الدم مما يجعل المريض يشعر بالإرهاق.
وطُوّر علاج كاسجيفي، الذي يتم يتسويقه حالياً باسم “ليفجينيا”، من مختبرات “فيرتكس فارماسوتيكلز الأميركية وشركة “كريسبر ثيربابوتيكس” السويسرية الأميركية، لعلاج المرضى الذين يعانون من اثنين من أخطر أمراض الدم الوراثية النادرة: فقر الدم المنجلي والثلاسيميا بيتا.
وكانت السلطات الصحية البريطانية أول من وافق على استخدامه لهذين المرضين في نوفمبر 2023. وحذت نظيراتها الأميركية والأوروبية والسعودية حذوها هذا العام. كما نشرت المفوضية الأوروبية قرارها بشأن ترخيص طرح هذا العلاج في الأسواق في 12 فبراير الماضي.
◙ العلاجات السابقة لم تستطع أن تحد من المشاكل التي يعاني منها مرضى الثلاسيميا كهشاشة العظام وتليف الكبد
والتلاسيميا ومرض الخلايا المنجلية من أمراض الدم الوراثية. حيث ينخفض نتاج الهيموجلوبين لدى مرضى الثلاسيميا بيتا، مما يؤدي إلى انخفاض عدد خلايا الدم الحمراء مع أعراض مثل التعب وضيق التنفس وعدم انتظام ضربات القلب.
فيما يتعلق بفقر الدم المنجلي فهو مرض وراثي، يصيب حوالي 100 ألف شخص في الولايات المتحدة و20 مليون شخص في جميع أنحاء العالم. حيث ينتج الجسم الهيموجلوبين المعيب بدلاً عن السليم الذي يمكن أن يتكتل ويسد الأوعية الدموية، مما يقلل من إمدادات الأكسجين إلى الأنسجة ويؤدي إلى أزمة انسداد الأوعية الدموية. وتتطور أعراضه لتشمل فقر الدم، نوبات الألم، تلف الأعضاء، وصولاً إلى الوفاة المبكرة.
ويعتقد العلماء أن الأشخاص ذوي البشرة السوداء أكثر عرضةً للإصابة بهذا المرض، ويعزون ذلك إلى سمة الخلية المنجلية لديهم والتي تحمي من الملاريا.
ويعتبر مقص “كريسبر” الجزيئي أو تقنية “كريسبر”(تقنية تحرير الجينات)، ثورة في عالم العلاج باستخدام الخلايا الجذعية تم اكتشافها في عام 2012، من قبل الفرنسية إيمانويل شاربنتييه والأميركية جنيفر دودنا، الحائزتين على جائزة نوبل للكيمياء لعام 2020.
وتعمل التقنية على تعديل المورث المعيب للمريض، وتعديل الخلايا المريضة وراثياً باستخدام فيروس غير ضار لحمل نسخة صحية من المورث الذي ينتج الهيموغلوبين إلى الخلايا. ويقوم الأطباء أولاً بتجميع الخلايا الجذعية للمريض. ثم يأتي الجزء الصعب، المتمثل في إزالة الخلايا الجذعية من الحبل الشوكي للمريض من طريق العلاج الكيميائي، ما يفسح المجال للخلايا المعدّلة.
ويعاب على هذه التقنية أنّ 88 في المئة من العلاجات المرتبطة بها هي في مراحل مبكرة من التطوير، كما تتطلب استثمارات ضخمة حيث يخضع كل مريض مشارك في التجربة السريرية لمتابعة تستمر 15 عاماً. هذا بالإضافة إلى تكلفتها الباهظة التي تصل إلى 3.1 ملايين دولار للمريض الواحد.
ويعلّق البروفيسور سيمون وادينغتون، المتخصص في العلاج الجيني في جامعة "يونيفرسيتي كولدج لندن" على ذلك "لن يكون ممكنا توفير هذا العلاج في البلدان المنخفضة والمتوسطة الدخل"، مضيفا إنه "ليس دواء يمكن حقنه بسهولة أو تناوله في شكل حبوب".
ويرى الكثير من علماء الوراثة والأمراض في هذا العلاج الجديد بارقة أمل تفتح أبواب أمام ثورة العلاج الجيني، كما انّ التراخيص التي منحت لعلاج كريسبر "تفتح الباب أمام تطبيقات أخرى لعلاجات كريسبر في المستقبل لمداواة الكثير من الأمراض الوراثية والمكتسبة ومنها السرطان".




















